Chemia w Szkole

Sacharydy
Foto – Dreamstime
Nieco inaczej o sacharydach
dr Joanna Kurek
Cukierki, dropsy, pianki, czekoladki, landrynki, żelki, lizaki, a najlepiej cała ich góra to słodkości, którym trudno oprzeć się dzieciom, a zapewne i wielu dorosłym.
Podstawowe składniki słodyczy – węglowodany (sacharydy), takie jak sacharoza, glukoza czy fruktoza są substancjami głównie pochodzenia roślinnego, których pierwotnym źródłem jest fotosynteza. Szacuje się, iż w ciągu każdego roku na Ziemi, w wyniku procesu biosyntezy prowadzonej głównie przez rośliny, a także m. in. przez bakterie fotosyntetyzujące, glony czy grzyby powstaje około 4×1011 ton węglowodanów, przede wszystkim w postaci polisacharydów, odznaczających się ogromną różnorodnością struktur. Ich badania polegają na analizie połączeń poszczególnych ugrupowań monosacharydów, przy czym istnieją tu różne możliwości. Dwie takie same cząsteczki monosacharydu mogą utworzyć aż 11 disacharydów (dla porównania – istnieje tylko jedna możliwość połączenia dwóch cząsteczek tego samego aminokwasu). Cząsteczki 2 różnych monosacharydów można połączyć na 20 różnych sposobów (nie zmieniając wielkości ich pierścieni), podczas gdy 2 cząsteczki różnych aminokwasów można połączyć na 4 sposoby.
Celem niniejszego opracowania jest przedstawienie sacharydów przede wszystkim w ujęciu spożywczym oraz przedstawienie mniej znanych eksperymentalnych sposobów ich wykrywania, a także jakościowej oraz ilościowej analizy.
Cukry a węglowodany – na czym polega różnica?
Dla biochemika terminy: „węglowodany” i „sacharydy” to często synonimy. Jednak ze ściśle chemicznego punktu widzenia utożsamianie tych nazw nie jest zalecane z tego względu, iż wzory sumaryczne niektórych sacharydów nie odpowiadają wielokrotności ugrupowania C(HOH), mogąc mieć w swojej budowie np. grupy aminowe –NH2, co ma miejsce w chitynie, a także mogą tworzyć połączenia z peptydami, proteinami czy lipidami. Zatem najbardziej ogólna nazwa, obejmująca różne warianty omawianych tu związków to sacharydy.
Jeden z możliwych podziałów sacharydów, wyróżniający cukry proste (monosacharydy) i złożone (oligosacharydy i polisacharydy), co wynika z ich zdolności do kondensacji (polimeryzacji), pokazany został na Rys 1.
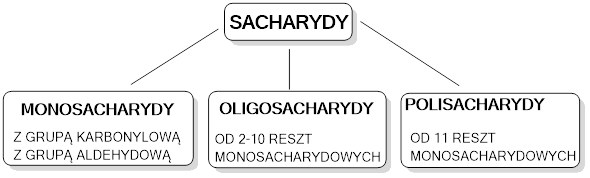
Rys. 1. Podział sacharydów.
Z kolei w języku potocznym słów takich jak cukry i węglowodany najczęściej używa się zamiennie, choć nie są to, ściśle rzecz biorąc, synonimy. Świadczą o tym choćby etykiety produktów spożywczych, podające ich skład w postaci „węglowodany, w tym cukry”. W istocie pojęcie ‘węglowodanów’ jest z kolei szersze niż ‘cukrów’. W tym ujęciu „węglowodany” oznaczają bowiem całkowitą zawartość substancji o charakterze sacharydów, natomiast określenie ‘cukry’ jest używane do ujęcia wyłącznie mono- i disacharydów w żywności. Zdarza się, że w niektórych produktach spożywczych zawartość węglowodanów pokrywa się z zawartością cukrów, tak jak np. w dżemach. Poza tym, w składzie niektórych produktów spożywczych, w obrębie węglowodanów wyszczególnione są też ‘poliole’, czyli alkohole polihydroksylowe odznaczające się słodkim smakiem, takie jak: ksylitol, maltitol czy erytrol (erytrytol).
Właściwości fizyczne i chemiczne sacharydów
Sacharydy różnią się m. in. rozpuszczalnością w wodzie i stopniem ich słodkości, co ma istotne znaczenie dla wykorzystania tych związków jako składników żywności. W szczególności monosacharydy są zwykle rozpuszczalne w wodzie i wykazują słodki smak. Polisacharydy natomiast nie wykazują słodkiego smaku, są słabiej lub wręcz praktycznie nierozpuszczalne w wodzie, odznaczając się przy tym zróżnicowanymi masami cząsteczkowymi.
Szczególnym procesem, jakiemu ulegają monosacharydy w wodnych roztworach jest mutarotacja, podczas której następuje naprzemienne, tautomeryczne przekształcanie się anomeru α w anomer β i odwrotnie, eksperymentalnie obserwowalne przez zmianę wartości skręcalności optycznej roztworu, od czego pochodzi nazwa tego zjawiska. Proces ten zachodzi poprzez formę łańcuchową z udziałem anomerycznego atomu węgla. Specyficzne właściwości monosacharydy zawdzięczają także grupie aldehydowej, która może zostać utleniona lub zredukowana. Produktami redukcji są poliole (np. redukcja D-fruktozy prowadzi do uzyskania D-glucitolu (sorbitolu) i D-mannitolu).
Reakcje redukcji grupy aldehydowej znalazły zastosowanie m.in. w reakcjach wykrywania cukrów za pomocą dobrze znanych prób, np. Tollensa czy Trommera. Z kolei grupy hydroksylowe w sacharydach ulegają rożnym reakcjom: estryfikacji, dehydratacji czy też wytworzeniu wiązań O-glikozydowych oraz biorą udział w tworzeniu związków kompleksowych z jonami metali, co ma także znaczenie w reakcjach wykrywania cukrów. Estryfikacja sacharydów obejmuje reakcje z organicznymi bezwodnikami kwasowymi, kwasami nieorganicznymi, chlorkami arylowymi. W reakcjach z wyższymi kwasami tłuszczowymi mogą brać udział mono-, di-, oligosacharydy czy nawet alkohole sacharydowe, w wyniku czego powstają związki powierzchniowo czynne, istotne w produkcji żywności.
Podczas ogrzewania monosacharydów w temperaturze wyższej niż temperatura topnienia zachodzi ich dehydratacja, polegająca początkowo na odwracalnym wydzieleniu cząsteczki wody, ale przy dalszym prowadzeniu tego procesu powstają produkty o wyższym stopniu odwodnienia, stanowiące przejaw karmelizacji sacharydów.
Ciekawym aspektem jest też higroskopijność sacharydów, czego szczególnym przykładem jest zmiana zachodząca w przypadku sacharozy (rozdrobnionej – cukier puder) pod wpływem wilgoci z powietrza, czego nie obserwuje się dla glukozy czy też fruktozy, będących dwoma monosacharydami budującymi disacharyd sacharozę.
Cały artykuł dr Joanny Kurek przeczytacie w wydaniu 5/2023 „Chemii w Szkole”.
